Peptide-ähnlech Synthesetechnologie
D'Fuerschung an d'Entwécklung vu Peptidmedikamenter wiisst séier an der Medizin.Wéi och ëmmer, d'Entwécklung vu Peptidmedikamenter ass limitéiert duerch hir eege Charakteristiken.Zum Beispill, wéinst der spezieller Empfindlechkeet fir enzymatesch Hydrolyse, gëtt d'Stabilitéit reduzéiert, an d'Verännerlechkeet vun der sterescher Konformatioun resultéiert zu enger gerénger Zilspezifizitéit, enger gerénger Hydrophobitéit an engem Mangel un engem spezifesche Transportsystem.Fir dës Peptiden ze iwwerwannen, proposéiert vill Léisungen an erfollegräich Uwendung vun enger Aart vu Peptid ass ee vun hinnen.
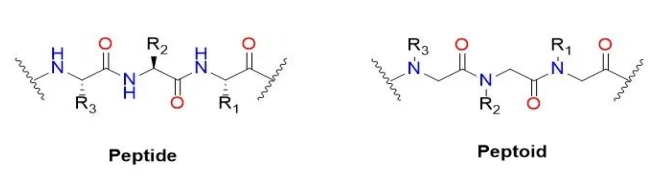
Aart vu Peptid (engleschen Numm: Peptoid) oder Poly - N - amplaz Glycin (engleschen Numm: Poly real - N - substitutedglycine), et ass e quasi Peptidverbindunge vu Peptid an der Haaptkette.D'Alpha Kuelestoff Säit Kette transferéiert d'Haaptkette Stickstoff amplaz vun der Säit Kette.Am ursprénglechen Polypeptid representéiert d'R Grupp vun der Aminosaier Säitkette 20 verschidden Aminosäuren, awer d'R Grupp huet méi Optiounen am Peptoid.Am Peptid, Peptid op der Haaptkette vun Aminosäuren am Alpha Kuelestoff Stickstoff amplaz Säit Kette Transfert an d'Haaptkette.Et ass derwäert ze erwähnen datt Peptiden am Allgemengen net déiselwecht héich-Niveau bestallte Strukturen produzéieren wéi sekundär Strukturen a Peptiden a Proteinen wéinst dem Mangel u Waasserstoff um Réckemuerch Stickstoff.Peptid initial Zweck ass stabil a Protease Peptid vu klenge Molekül Drogen z'entwéckelen.
Analyse vu peptidähnleche Synthesetechniken
D'Method vun der Peptidsynthese gouf agefouert
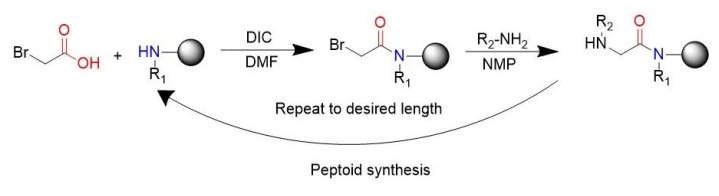
Déi allgemeng populär peptidähnlech Synthesemethod ass déi subsingle Synthesemethod erfonnt vum RonZuckermann, déi jidderee an zwee Schrëtt opgedeelt ass: Acylatioun an Verschiebung.An der Acylatioun ass den éischte Schrëtt d'Haloediksäure ze aktivéieren fir mat den Aminen ze reagéieren déi um Enn vum virege Schrëtt bleiwen, am meeschten diisopropyl karboniséierter Diimin.bromoaceticacid war vun diisopropylcarbodiimid aktivéiert."A Substitutiounsreaktiounen (bimolekulär nukleophil Substitutiounsreaktiounen) attackéiert en Amin, typesch primär, den alternativen Halogen fir en N-substituéiert Glycin ze bilden."Déi subunitär synthetesch Streck benotzt einfach verfügbar primär Amine fir Peptiden ze generéieren, an doduerch d'chemesch Synthese vu Peptiden z'erméiglechen.
Solid Extensioun an der Klass Peptidsynthese huet déi räich Erfahrung, kann Iech eng Vielfalt vun Aarte vu Peptidsyntheseservice ubidden.
Analyse vu peptidähnleche Synthesetechniken
De Virdeel vun esou Peptid
Méi stabil: Peptoide si méi stabil in vivo wéi Peptiden.
Méi Selektivitéit: Peptoide si gutt gëeegent fir kombinéiert Medikamententdeckungsstudien, well eng grouss Varietéit vu verschiddene Polypeptid Bausteng kann duerch Modifikatioun vun der Backbone Aminogrupp kritt ginn.
Méi effizient: D'Heefegkeet vu peptoid Strukturen kann Peptoid eng gutt Wiel fir Scannen Methodik maachen fir séier spezifesch Strukturen ze fannen, déi un Proteinen binden.
Méi Maartpotenzial: d'Charakteristike vun der Aart vu Peptid léisst et eng Aart vun Drogenentwécklung ginn huet e grousst Potenzial.
Post Zäit: Dez-07-2023