Peptiden sinn eng Klass vu Verbindunge geformt duerch d'Verbindung vu multiple Aminosäuren duerch Peptidbindungen.Si sinn ubiquitär a liewegen Organismen.Bis elo sinn Zéngdausende vu Peptiden a liewegen Organismen fonnt ginn.Peptiden spillen eng wichteg Roll bei der Reguléierung vun der funktionell Aktivitéite vu verschiddene Systemer, Organer, Stoffer an Zellen a Liewensaktivitéiten, a ginn dacks a funktionell Analyse, Antikörperfuerschung, Drogenentwécklung an aner Felder benotzt.Mat der Entwécklung vu Biotechnologie a Peptidsynthesetechnologie sinn ëmmer méi Peptidmedikamenter an der Klinik entwéckelt an applizéiert ginn.
Et ginn eng breet Varietéit vu Peptidmodifikatioune, déi einfach a Postmodifikatioun a Prozessmodifikatioun ënnerdeelt kënne ginn (mat ofgeleet Aminosaier Modifikatioun), an N-terminal Modifikatioun, C-terminal Modifikatioun, Säitekette Modifikatioun, Aminosaier Modifikatioun, Skelett Modifikatioun, etc., jee no der Modifikatiounsplaz (Figur 1).Als e wichtegt Mëttel fir d'Haaptkettestruktur oder Säitekettengruppen vu Peptidketten z'änneren, kann d'Peptidmodifikatioun effektiv d'physikalesch a chemesch Eegeschafte vu Peptidverbindungen änneren, d'Waasserléislechkeet erhéijen, d'Aktiounszäit in vivo verlängeren, hir biologesch Verdeelung änneren, d'Immunogenizitéit eliminéieren. , reduzéieren gëfteg Säit Effekter, etc.. An dësem Pabeier, puer grouss Peptid Modifikatioun Strategien an hir Charakteristiken agefouert.
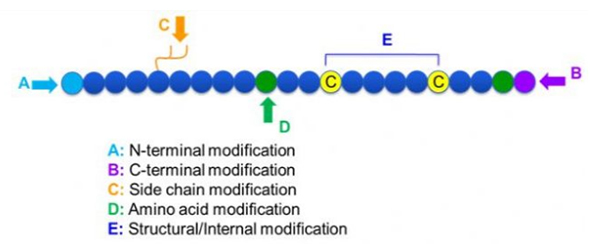
1. Cyclisatioun
Cyclesch Peptiden hu vill Uwendungen an der Biomedizin, a vill natierlech Peptiden mat biologescher Aktivitéit si zyklesch Peptiden.Well zyklesch Peptiden éischter méi steif sinn wéi linear Peptiden, si si extrem resistent géint den Verdauungssystem, kënnen am Verdauungstrakt iwwerliewen an eng méi staark Affinitéit fir Zilrezeptoren weisen.Cyclisatioun ass den direktste Wee fir zyklesch Peptiden ze synthetiséieren, besonnesch fir Peptiden mat grousse strukturelle Skelett.Geméiss dem Cyclisatiounsmodus kann et opgedeelt ginn op Säitketten-Säit Kettentyp, Terminal - Säitkettentyp, Terminal - Terminaltyp (Enn bis Enn Typ).
(1) sidechain-zu-sidechain
Déi heefegst Aart vu Säitekette zu Säitekette Cyclisatioun ass Disulfid Bréckung tëscht Cysteinreschter.Dës Cyclisatioun gëtt duerch e Paar Cysteinreschter agefouert, déi ofgeschützt ginn an dann oxidéiert ginn fir Disulfidbindungen ze bilden.Polyzyklesch Synthese kann duerch selektiv Entfernung vu Sulfhydryl-Schutzgruppen erreecht ginn.Cyclisatioun kann entweder an engem Post-Dissoziatiounsléisungsmëttel oder op engem Pre-Dissoziatiounsharz gemaach ginn.Cyclisatioun op Harze ka manner effektiv sinn wéi Léisungsmëttelzyklus well d'Peptiden op Harze net einfach cyclifizéiert Konformatiounen bilden.Eng aner Aart vu Säiteketten-Säitkette Cyclisatioun ass d'Bildung vun enger Amidestruktur tëscht enger Asparaginsäure oder Glutaminsäurereschter an der Basis Aminosäure, déi erfuerdert datt d'Säitkette Schutzgrupp muss selektiv aus dem Polypeptid entweder geläscht ginn. op der Harz oder no der Dissoziatioun.Déi drëtt Zort vun Säit-Kette - Säit Kette Cyclisatioun ass d'Bildung vun Diphenylethers duerch Tyrosin oder p-Hydroxyphenylglycine.Dës Aart vu Cyclisatioun an natierleche Produkter gëtt nëmme a mikrobielle Produkter fonnt, a Cyclisatiounsprodukter hunn dacks potenziell medizinesche Wäert.D'Virbereedung vun dëse Verbindungen erfuerdert eenzegaarteg Reaktiounsbedéngungen, sou datt se net dacks an der Synthese vu konventionelle Peptiden benotzt ginn.
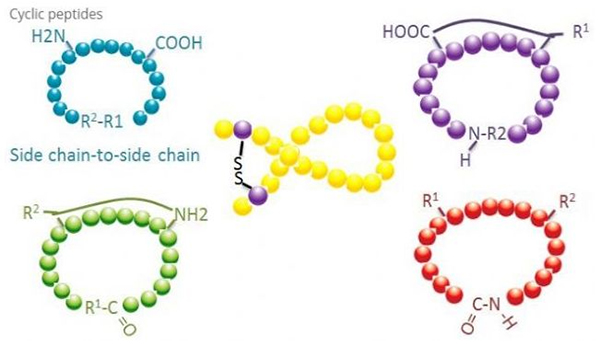
(2) terminal-zu-sidechain
Terminal-Säit-Kette Cyclization involvéiert normalerweis den C-Terminal mat der Aminogrupp vun der Lysin oder Ornithine Säit Kette, oder den N-Terminal mat der Asparaginsäure oder Glutaminsäure Säit Kette.Aner Polypeptid Zyklizéierung gëtt gemaach andeems Etherbindungen tëscht Terminal C a Serin oder Threonin Säitketten bilden.
(3) Terminal oder Kapp-ze-Schwanz Typ
Kette Polypeptide kënnen entweder an engem Léisungsmëttel zyklen oder op engem Harz fixéiert ginn duerch Säitkette Cyclation.Niddereg Konzentratioune vu Peptiden sollten an der Léisungsmëttelzentraliséierung benotzt ginn fir Oligomeriséierung vu Peptiden ze vermeiden.D'Ausbezuelung vun engem Kapp-zu-Schwanz syntheteschen Ringpolypeptid hänkt vun der Sequenz vum Kettepolypeptid of.Dofir, ier Dir zyklesch Peptiden op enger grousser Skala virbereet, sollt eng Bibliothéik vu méigleche chained Lead Peptiden als éischt erstallt ginn, gefollegt vun der Cyclisatioun fir d'Sequenz mat de beschten Resultater ze fannen.
2. N-methylation
N-Methylatioun geschitt ursprénglech an natierleche Peptiden a gëtt an d'Peptidsynthese agefouert fir d'Bildung vu Waasserstoffbindungen ze vermeiden, wouduerch Peptiden méi resistent géint Biodegradatioun a Clearance maachen.Synthese vu Peptiden mat N-methyléierten Aminosaier Derivate ass déi wichtegst Method.Zousätzlech kann d'Mitsunobu-Reaktioun vun N-(2-Nitrobenzen-Sulfonylchlorid) Polypeptid-Harz Zwëscheprodukter mat Methanol och benotzt ginn.Dës Method gouf benotzt fir zyklesch Peptidbibliothéike mat N-methyléierten Aminosaieren ze preparéieren.
3. Phosphorylatioun
Phosphorylatioun ass eng vun den heefegste post-translational Ännerungen an der Natur.A mënschlechen Zellen si méi wéi 30% vun Proteinen phosphoryléiert.Phosphorylatioun, besonnesch reversibel Phosphorylatioun, spillt eng wichteg Roll bei der Kontroll vu ville celluläre Prozesser, wéi Signaltransduktioun, Genausdrock, Zellzyklus an Zytoskelettreguléierung, an Apoptose.
Phosphorylatioun ka bei enger Vielfalt vun Aminosaierreschter observéiert ginn, awer déi heefegst Phosphorylatiounsziler si Serin, Threonin an Tyrosinreschter.Phosphotyrosin, Phosphothreonin, a Phosphoserin Derivate kënnen entweder a Peptiden während der Synthese agefouert ginn oder no der Peptidsynthese geformt ginn.Selektiv Phosphorylatioun kann erreecht ginn mat Iwwerreschter vu Serin, Threonin an Tyrosin, déi selektiv Schutzgruppen entfernen.E puer Phosphorylatiounsreagenz kënnen och Phosphorsäuregruppen an d'Polypeptid duerch Postmodifikatioun aféieren.An de leschte Jore gouf Site-spezifesch Phosphorylatioun vu Lysin mat enger chemesch selektiv Staudinger-Phosphitreaktioun erreecht (Figur 3).
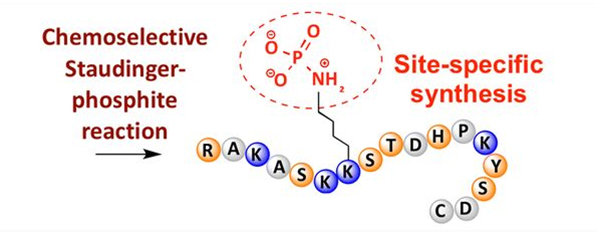
4. Myristoylatioun a Palmitoylatioun
Acylatioun vum N-Terminal mat Fettsäuren erlaabt Peptiden oder Proteinen un Zellmembranen ze binden.Déi myridamoyléiert Sequenz um N-Terminal erméiglecht d'Src Famill Proteinkinasen a Reverse Transkriptase Gaq Proteine ze zielen fir un Zellmembranen ze binden.Myristinsäure gouf mam N-Terminal vum Harz-Polypeptid mat Hëllef vu Standardkupplungsreaktiounen verbonnen, an dat entstinn Lipopeptid konnt ënner Standardbedéngungen dissoziéiert ginn an duerch RP-HPLC gereinegt ginn.
5. Glycosylatioun
Glycopeptide wéi Vancomycin an Teicolanin si wichteg Antibiotike fir d'Behandlung vun Drogen-resistente bakterielle Infektiounen, an aner Glycopeptide ginn dacks benotzt fir den Immunsystem ze stimuléieren.Zousätzlech, well vill mikrobiell Antigene glycosyléiert sinn, ass et vu grousser Bedeitung Glycopeptide ze studéieren fir den therapeuteschen Effekt vun der Infektioun ze verbesseren.Op der anerer Säit ass et fonnt ginn datt d'Proteine op der Zellmembran vun Tumorzellen anormal Glykosylatioun weisen, wat Glycopeptide mécht eng wichteg Roll bei Kriibs an Tumor Immunverteidegungsfuerschung ze spillen.Glycopeptide ginn duerch Fmoc / t-Bu Method virbereet.Glycosyléiert Reschter, wéi Threonin a Serin, ginn dacks a Polypeptide agefouert duerch pentafluorophenolester aktivéiert fMOCs fir glycosyléiert Aminosäuren ze schützen.
6. Isopren
Isopentadienylatioun geschitt op Cysteinreschter an der Säitekette bei der C-Terminal.Protein Isopren kann d'Zellmembranaffinitéit verbesseren a Protein-Protein Interaktioun bilden.Isopentadienéiert Proteinen enthalen Tyrosinphosphatase, kleng GTase, Cochaperone Moleküle, nuklear Lamina, an centromeresch Bindungsproteine.Isopren Polypeptide kënne mat Isopren op Harze virbereet ginn oder andeems Cystein Derivate agefouert ginn.
7. Polyethylenglycol (PEG) Modifikatioun
PEG Modifikatioun ka benotzt ginn fir d'Protein hydrolytesch Stabilitéit, d'Bioverdeelung an d'Peptidléislechkeet ze verbesseren.D'Aféierung vu PEG Ketten op Peptiden kann hir pharmakologesch Eegeschafte verbesseren an och d'Hydrolyse vu Peptiden duerch proteolytesch Enzyme hemmen.PEG Peptiden passéieren duerch de glomeruläre Kapillar Querschnëtt méi einfach wéi gewéinlech Peptiden, wat d'Nier Clearance staark reduzéiert.Wéinst der erweiderter aktiver Hallefzäit vu PEG-Peptiden in vivo kann den normale Behandlungsniveau mat méi nidderegen Dosen a manner dacks Peptid-Drogen erhale ginn.Wéi och ëmmer, PEG Modifikatioun huet och negativ Auswierkungen.Grouss Quantitéite vu PEG verhënneren datt den Enzym de Peptid ofbaut an och d'Bindung vum Peptid un den Zilrezeptor reduzéieren.Awer d'niddereg Affinitéit vun PEG Peptiden gëtt normalerweis duerch hir méi laang pharmakokinetesch Hallefzäit kompenséiert, a andeems se méi laang am Kierper präsent sinn, hunn PEG Peptiden eng méi grouss Wahrscheinlechkeet fir an Zilgewebe absorbéiert ze ginn.Dofir sollten PEG Polymer Spezifikatioune fir optimal Resultater optimiséiert ginn.Op der anerer Säit accumuléieren PEG-Peptiden an der Liewer wéinst reduzéierter Nierklärung, wat zu makromolekuläre Syndrom resultéiert.Dofir musse PEG Modifikatioune méi suergfälteg entworf ginn wann Peptiden fir Drogentest benotzt ginn.
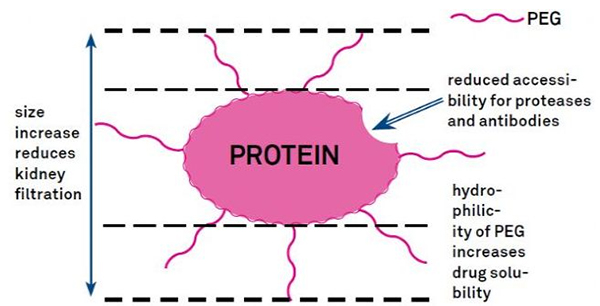
Gemeinsam Modifikatiounsgruppen vu PEG Modifizéierer kënnen ongeféier wéi follegt zesummegefaasst ginn: Amino (-amine) -NH2, Aminomethyl-Ch2-NH2, Hydroxy-OH, Carboxy-Cooh, Sulfhydryl (-Thiol) -SH, Maleimid -MAL, Succinimidkarbonat - SC, succinimidacetat -SCM, succinimidpropionat -SPA, n-hydroxysuccinimid -NHS, Acrylat-ch2ch2cooh, aldehyd -CHO (wéi propional-ald, butyrALD), acrylbase (-acrylat-acrl), azido-azid, biotinyl - Biotin, Fluorescein, Glutaryl -GA, Acrylat Hydrazid, Alkyn-Alkyn, p-Toluensulfonat -OTs, Succinimid-Succinat -SS, etc. PEG-Derivate mat Carboxylsäuren kënne mat n-terminalen Aminen oder Lysin-Säitketten gekoppelt ginn.Amino-aktivéiert PEG kann un Asparaginsäure oder Glutaminsäure Säitkette gekoppelt ginn.Mal-ageschalt PEG kann zu mercaptan vun voll deprotected cysteine Säit Ketten conjugated ginn [11].PEG Modifikateure ginn allgemeng wéi follegt klasséiert (Notiz: mPEG ass Methoxy-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) riichtaus Kette PEG Modifier
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2) bifunktionelle PEG-Modifier
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) branching PEG Modifier
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Biotiniséierung
Biotin ka staark mat Avidin oder Streptavidin gebonnen ginn, an d'Bindungsstäerkt ass souguer no bei der kovalenter Bindung.Biotin-labeléiert Peptiden ginn allgemeng an Immunoassay, Histocytochemie a Fluoreszenz-baséiert Flowzytometrie benotzt.Labeléiert Antibiotin Antikörper kënnen och benotzt ginn fir biotinyléiert Peptiden ze binden.Biotin Etiketten ginn dacks un der Lysin Säit Kette oder dem N Terminal befestegt.6-Aminokapronsäure gëtt dacks als Bindung tëscht Peptiden a Biotin benotzt.D'Bindung ass flexibel an der Bindung un de Substrat a bindt besser a Präsenz vu steresche Hindernisser.
9. Fluorescent Etikettéierung
Fluoreszent Etikettéiere kënne benotzt ginn fir Polypeptiden a liewegen Zellen ze verfolgen an Enzymen a Mechanismen vun der Handlung ze studéieren.Tryptophan (Trp) ass fluoreszent, sou datt et fir intrinsesch Label benotzt ka ginn.Den Emissiounsspektrum vum Tryptophan hänkt vum periphere Ëmfeld of a fällt mat erofgaang Léisungsmëttelpolaritéit, eng Eegeschafte déi nëtzlech ass fir Peptidstruktur an Rezeptorbindung z'entdecken.Tryptophan Fluoreszenz kann duerch protonéiert Asparaginsäure a Glutaminsäure geläscht ginn, wat seng Notzung limitéiere kann.D'Dansylchloridgrupp (Dansyl) ass héich fluoreszent wann se un eng Aminogrupp gebonnen ass a gëtt dacks als fluoreszent Label fir Aminosäuren oder Proteinen benotzt.
Fluoreszenz Resonanz Energie Konversioun (FRET) ass nëtzlech fir Enzym Studien.Wann FRET applizéiert gëtt, enthält de Substrat Polypeptid normalerweis eng Fluoreszenz-Labelgrupp an eng Fluoreszenz-Quenching-Grupp.Labeléiert fluoreszent Gruppe gi vum Quencher duerch net-Photonenergietransfer ofgeschwächt.Wann de Peptid vum Enzym a Fro dissoziéiert ass, emittéiert d'Etikettéierungsgrupp Fluoreszenz.
10. Cage polypeptides
Cage Peptiden hunn optesch eraushuelbare Schutzgruppen, déi d'Peptid aus der Bindung un den Rezeptor schützen.Wann UV-Bestrahlung ausgesat ass, gëtt de Peptid aktivéiert, a seng Affinitéit zum Rezeptor restauréiert.Well dës optesch Aktivatioun no Zäit, Amplitude oder Standuert kontrolléiert ka ginn, kënne Käfegpeptide benotzt ginn fir Reaktiounen ze studéieren déi an Zellen optrieden.Déi meescht benotzt Schutzgruppen fir Käfegpolypeptide sinn 2-Nitrobenzylgruppen an hir Derivate, déi an der Peptidsynthese iwwer schützend Aminosaier Derivate agefouert kënne ginn.Aminosaier Derivate, déi entwéckelt goufen, sinn Lysin, Cystein, Serin, an Tyrosin.Aspartat a Glutamat Derivate ginn awer net allgemeng benotzt wéinst hirer Empfindlechkeet fir Cycliséierung wärend der Peptidsynthese an der Dissoziatioun.
11. Polyantigenic Peptid (MAP)
Kuerz Peptiden sinn normalerweis net immun a mussen un Trägerproteine gekoppelt ginn fir Antikörper ze produzéieren.Polyantigenic Peptid (MAP) besteet aus multiple identesche Peptiden verbonne mat Lysin Käre, déi speziell héich Potenz Immunogene ausdrécke kënnen a kënne benotzt ginn fir Peptid-Träger Proteincouplets ze preparéieren.MAP Polypeptide kënnen duerch zolidd Phase Synthese op MAP Harz synthetiséiert ginn.Wéi och ëmmer, onvollstänneg Kupplung resultéiert zu fehlend oder ofgeschniddene Peptidketten op e puer Filialen a weist also net d'Eegeschafte vum originelle MAP Polypeptid.Als Alternativ kënnen Peptiden getrennt virbereet a gereinegt ginn an dann un MAP gekoppelt ginn.D'Peptid Sequenz, déi un de Peptidkär befestegt ass, ass gutt definéiert a liicht duerch Massespektrometrie charakteriséiert.
Conclusioun
Peptidmodifikatioun ass e wichtegt Mëttel fir Peptiden ze designen.Chemesch modifizéiert Peptiden kënnen net nëmmen eng héich biologesch Aktivitéit erhalen, awer och effektiv d'Nodeeler vun der Immunogenizitéit an der Toxizitéit vermeiden.Zur selwechter Zäit kann chemesch Modifikatioun Peptiden mat e puer nei exzellenten Eegeschafte ginn.An de leschte Joeren ass d'Methode vun der CH Aktivéierung fir d'Postmodifikatioun vu Polypeptiden séier entwéckelt ginn, a vill wichteg Resultater goufen erreecht.
Post Zäit: Mar-20-2023
